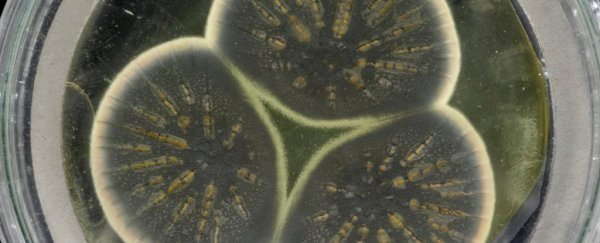
 Alexander Flemings Penicillium rubens, von den Toten auferweckt. (CABI)
Alexander Flemings Penicillium rubens, von den Toten auferweckt. (CABI) Im Jahr 1928 schrieb der schottische Wissenschaftler Alexander Fleming Geschichte. In einem gewöhnlichen Schimmelpilz – so häufig, dass der Stamm zufällig in einer Petrischale wuchs Staphylokokken - er entdeckte antimikrobielle Eigenschaften, die er nutzen würde, um das erste massenproduzierte Antibiotikum zu entwickeln, Penicillin .
Das Originalstamm von Penicillium Schimmel wurde vor Jahrzehnten kryogen konserviert – für die Nachwelt lebendig eingefroren –, doch jetzt wurde zum ersten Mal sein Genom sequenziert. Und ähnlich wie die Entdeckung von Penicillin selbst entwickelte sich die Forschung als Ableger von etwas anderem.
„Ursprünglich hatten wir vor, den Pilz von Alexander Fleming für verschiedene Experimente zu verwenden.“ erklärte der Evolutionsbiologe Timothy Barraclough des Imperial College London und der Universität Oxford. „Aber zu unserer Überraschung stellten wir fest, dass niemand das Genom dieses Originals sequenziert hatte Penicillium , trotz seiner historischen Bedeutung für das Fachgebiet.'
Die neu abgeleitete Sequenz wurde mit zwei späteren, kommerziell hergestellten Sequenzen verglichen Penicillium Genomen aus den USA, die es Forschern ermöglichen, zu sehen, wie die Produktion im industriellen Maßstab die genetische Ausstattung des Schimmelpilzes im Laufe der Zeit und über Entfernungen leicht verändert hat.
Penicillium und andere Schimmelpilze produzieren auf natürliche Weise Antibiotikamoleküle als Teil ihres eigenen Abwehrsystems gegen Mikroben. Da sich Mikroben recht schnell weiterentwickeln, um diesen Abwehrkräften entgegenzuwirken – eine Eigenschaft, die derzeit ein ziemliches Problem in Form von… darstellt Antibiotikaresistenz - Auch Formen entwickeln sich als Reaktion darauf.
Auf mikroskopischer Ebene gleicht es einem Wettrüsten, und die genaue Untersuchung der Entwicklung der Schimmelpilze könnte neue Erkenntnisse über das heutige Problem der Antibiotikaresistenz liefern.
„Unsere Forschung könnte dazu beitragen, neue Lösungen zur Bekämpfung von Antibiotikaresistenzen zu entwickeln“, sagte der Biologe Ayush Pathak des Imperial College London.
Um ihre Forschung durchzuführen, taute das Team eine Probe von Fleming auf Ein roter Pinsel , und ließ es wieder wachsen. Von diesem frisch gewachsenen Schimmelpilz wurden dann Proben genommen und sequenziert. Das resultierende Genom wurde dann mit den US-Stämmen verglichen.
Flemings Penicillium war vielleicht der Begründer der Penicillin-Medikamente in Großbritannien, aber in den USA begann die industrielle Produktion mit einem wilden Isolat aus einer schimmeligen Melone. Dieser Stamm wurde mutagenen Behandlungen wie Bestrahlung mit Röntgen- und Ultraviolettlicht sowie künstlicher Selektion unterzogen, um einen Stamm mit hohen Penicillin-Produktionsraten zu erzeugen.
Jegliche Unterschiede zwischen dem Fleming-Schimmelpilz und dem US-Schimmelpilz sind entweder das Ergebnis evolutionärer Unterschiede im wilden Cantaloupe-Stamm oder die frühen Schritte der Mutagenese und künstlichen Selektion.
Beim Vergleich untersuchten die Forscher zwei Arten von Genen – diejenigen, die die Enzyme kodieren, die bei der Penicillinproduktion helfen, und diejenigen, die die Produktion derselben Enzyme regulieren.
Es stellte sich heraus, dass der Fleming-Schimmelpilz und der US-Schimmelpilz im Wesentlichen den gleichen genetischen Code für die regulatorischen Enzyme haben. Interessanterweise hatte der US-Schimmelpilz mehr Kopien – was diesen Stämmen helfen würde, mehr Penicillin zu produzieren.
Das ist nicht überraschend, da sie speziell für diesen Zweck gezüchtet wurden, aber es gibt einen Einblick in die Ergebnisse des Domestizierungsprozesses.
Die kodierenden Gene unterschieden sich jedoch geringfügig zwischen Flemings britischem Stamm und den US-Stämmen. Das Team geht davon aus, dass dies das Ergebnis einer natürlichen Evolution war, wahrscheinlich als Reaktion auf Unterschiede in den Mikroben, die die Schimmelpilze in ihrer lokalen Umgebung bedrohen.
Es ist dieser natürlich entstandene Unterschied, der ein Schlüssel zur Entwicklung von Lösungen für das Problem der Antibiotikaresistenz sein könnte.
„Die industrielle Produktion von Penicillin konzentrierte sich auf die produzierte Menge, und die Schritte zur künstlichen Verbesserung der Produktion führten zu Veränderungen in der Anzahl der Gene.“ sagte Pathak .
„Aber es ist möglich, dass industriellen Methoden einige Lösungen zur Optimierung des Penicillin-Designs entgangen sind, und wir können aus natürlichen Reaktionen auf die Entwicklung von Antibiotikaresistenzen lernen.“
Die Forschung wurde veröffentlicht in Wissenschaftliche Berichte .